रासायनिक अभिक्रियाएँ एवं समीकरण - क्लास दसवीं विज्ञान
Back to 10th-science-home(Hindi)
Balance Chemical Equation
संतुलित रासायनिक समीकरण
रासायनिक समीकरण, जिसमें दोनों ओर, अर्थात अभिकारकों के द्रव्यमान उत्पाद के द्रव्यमान के बराबर हो, उसे संतुलित रासायनिक समीकरण कहा जाता है।
दूसरे शब्दों में, रासायनिक समीकरण, जिसमें दोनों ओर, अर्थात अभिकारकों में तत्वों के परमाणुओं की संख्या उत्पाद के तत्वों के परमाणुओं की संख्या के बराबर हो, उसे संतुलित रासायनिक समीकरण कहा जाता है।
द्रव्यमान के संरक्षण के नियम के अनुसार रासायनिक प्रतिक्रिया में द्रव्यमान न तो बनता है और न ही उसका विनाश होता है।
इसका अर्थ है कि एक रासायनिक अभिक्रिया में अभिकारकों के रूप में वर्तमान तत्वों के परमाणुओं का द्रव्यमान उत्पाद के रूप में प्राप्त तत्वों के परमाणुओं के द्रव्यमान के बराबर होगा।
चूँकि सभी रासायनिक प्रतिक्रियाएँ; द्रव्यमान के संरक्षण के नियम का पालन करती हैं। अत: इस द्रव्यमान के नियम को संतुष्ट करने के लिए रासायनिक प्रतिक्रिया को दर्शाने के लिए लिखे गये रासायनिक समीकरण को संतुलित करना होता है।
रासायनिक समीकरण को कैसे संतुलित करें?
उदाहरण: मैग्निशियम के फीते का हवा में जलना।

इस दिये गये समीकरण, जो मैग्निशियम के फीते को हवा में जलने पर होने वाले रासायनिक प्रतिक्रिया को दर्शाता है, को निम्नांकित तरीके से संतुलित किया जा सकता है:
चरण (1) रासायनिक प्रतिक्रिया के लिए दिये गये रासायनिक समीकरण में वर्तमान सभी परमाणुओं की सख्याँ को एक टेबल में लिखें।
| दोनों तरफ परमाणुओं की संख्या | ||
|---|---|---|
| तत्व | प्रतिकारक (LHS) | उत्पाद (RHS) |
| Mg | 1 | 1 |
| O | 2 | 1 |
यहाँ, अभिकारक तथा उत्पाद दोनों में मैग्निशियम (Mg) की संख्या एक (1) है, अर्थात बराबर है।
अभिकारक में O2 (ऑक्सीजन) की संख्या दो (2) है, जबकि उत्पाद में इसकी संख्या एक (1) है।
अर्थात ऑक्सीजन की संख्या दिये गये रासायनिक समीकरण के दोनों पक्षों में बराबर नहीं है।
चरण (II) ऑक्सीजन की संख्या को संतुलित करने के लिये MgO (मैग्निशियम ऑक्साइड), जो उत्पाद है, को 2 (दो) से गुणा करें।
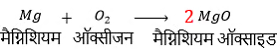
चरण (III) अब इस संशोधन के बाद इस रासायनिक समीकरण में अभिकारकों में तत्वों के परमाणु की संख्याओं को एक टेबल में लिखकर उसका आकलन करें।
| दोनों तरफ परमाणुओं की संख्या | ||
|---|---|---|
| तत्व | प्रतिकारक (LHS) | उत्पाद (RHS) |
| Mg | 1 | 2 |
| O | 2 | 2 |
अब संशोधन के पश्चात इस रासायनिक समीकरण में अभिकारक में मैग्निशियम के परमाणु की संख्या एक (1) है, तथा उत्पाद में मैग्निशियम के परमाणुओं की संख्या 2 (दो) हो गई है।
तथा, रासायनिक समीकरण में ऑक्सीजन की संख्या दोनों पक्षों, अर्थात बाएँ पक्ष और दाएँ पक्ष में दो (2) हो गयी है।
चरण (IV) रासायनिक समीकरण में मैग्निशियम की संख्या दोनों पक्षों में संतुलित करने के लिए प्रतिकारक में में वर्तमान Mg (मैग्निशियम) को दो (2) से गुणा करें।
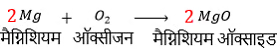
चरण (V) अब रासायनिक समीकरण में इस संशोधन के पश्चात फिर से, प्रतिकारक और उत्पाद में वर्तमान तत्वों के परमाणुओं की संख्या को एक टेबल में लिखें, तथा उसका आकलन करें।
| दोनों पक्षों में परमाणुओं की संख्या | ||
|---|---|---|
| तत्व | प्रतिकारक (LHS) | उत्पाद (RHS) |
| Mg | 2 | 2 |
| O | 2 | 2 |
अब, इस संशोधन के पश्चात मैग्निशियम के परमाणुओं की संख्या समीकरण के दोनों पक्षों में 2 (दो) हो गयी है, जो कि बराबर है।
तथा ऑक्सीजन (O2) के परमाणुओं की संख्या भी रासायनिक समीकरण में इस संशोधन के पश्चात प्रतिकारक और उत्पाद, दोनो पक्षों में 2 (दो) हो गयी है, जो कि बराबर है।
अब चूँकि रासायनिक समीकरण में इन संशोधनों के पश्चात दोनों पक्षों में वर्तमान तत्वों के परमाणुओं की संख्या बराबर हो गयी है, अत: दिया गया रासायनिक समीकरण संतुलित हो गया है।
उदाहरण: 2
जिंक की सल्फ्यूरिक अम्ल के साथ होने वाली प्रतिक्रिया के रासायनिक समीकरण को संतुलित करना
जब जिंक सल्फ्यूरिक अम्ल के साथ प्रतिक्रिया करता है, तो जिंक सल्फेट तथा हाइड्रोजन गैस बनती है।
जिंक + सल्फ्यूरिक अम्ल → जिंक सल्फेट + हाइड्रोजन
Zn⁄जिंक + H2SO4⁄सल्फ्यूरिक अम्ल → ZnSO4⁄जिंक सल्फेट + H2⁄हाइड्रोजन
जिंक तथा सल्फ्यूरिक अम्ल के बीच होने वाली प्रतिक्रिया के रासायनिक समीकरण को निम्नांकित रूप से संतुलित किया जा सकता है।
चरण (1) इस रासायनिक समीकरण के दोनों पक्षों अर्थात प्रतिकारक और उत्पाद में वर्तमान तत्वों के प्रमाणुओं की संख्या एक टेबल में लिखें।
| दोनों तरफ परमाणुओं की संख्या | ||
|---|---|---|
| तत्व | अभिकारक (LHS) | उत्पाद (RHS) |
| Zn | 1 | 1 |
| H | 2 | 2 |
| S | 1 | 1 |
| O | 4 | 4 |
इस टेबल के अवलोकन से यह स्पष्ट है कि दिये गये रासायनिक समीकरण के दोनों पक्षों अर्थात में अभिकारक और उत्पाद में वर्तमान सभी तत्वों की परमाणु की संख्या बराबर हैं। अत: दिया गया रासायनिक समीकरण संतुलित है।
उदाहरण: (3)
जब लोहा या लोहे से बनी वस्तुएँ लम्बे समय तक जल और हवा (ऑक्सीजन) के सम्पर्क में रहती है, जो उसमें जंग लग जाता है। जंग को अंग्रेजी में रस्ट (Rust) कहा जाता है। जंग का रासायनिक नाम आयरन (III) ऑक्साइड या फेरिक ऑक्साइड है, तथा इसका रासायनिक सूत्र Fe2O3 है।
अर्थात, जब लोहा जल से अभिक्रिया करता है, तो आयरन (III) ऑक्साइड और हाइड्रोजन गैस बनता है। इस प्रतिक्रिया को निम्नांकित रासायनिक समीकरण द्वारा दर्शाया जा सकता है।
Fe⁄आयरन + H2O⁄जल → Fe2O3⁄आयरन (III) ऑक्साइड + H2⁄हाइड्रोजन
चरण (1) इस रासायनिक समीकरण के दोनों पक्षों अर्थात प्रतिकारक और उत्पाद में वर्तमान तत्वों के प्रमाणुओं की संख्या एक टेबल में लिखें तथा परमाणुओं की संख्याओं का अवलोकन करें।
| दोनों पक्षों में परमाणुओं की संख्या | ||
|---|---|---|
| तत्व | अभिकारक (LHS) | उत्पाद (RHS) |
| Fe | 1 | 2 |
| H | 2 | 2 |
| O | 1 | 3 |
चरण (2) दिये गये रासायनिक समीकरण को संतुलित करने के लिए वैसा परमाणु जिसकी संख्या सबसे अधिक है, को सर्वप्रथम संतुलित करें।
टेबल के अवलोकन से स्पष्ट है कि उत्पाद में ऑक्सीजन की संख्या तीन (3) है, जबकि अभिकारक में ऑक्सीजन की संख्या एक है।
अत: ऑक्सीजन के परमाणुओं की संख्या को संतुलित करने के लिये अभिकारक में वर्तमान H2O (जल) को 3 (तीन) से गुणा करें।
Fe⁄आयरन + 3H2O⁄जल → Fe2O3⁄आयरन (III) ऑक्साइड + H2⁄हाइड्रोजन
चरण (3) अब इस संशोधित समीकरण के दोनों पक्षों में वर्तमान तत्वों के परमाणुओं की संख्या को पुन: एक टेबल में लिखकर उसका अवलोकन करें।
| दोनों पक्षों में परमाणुओं की संख्या | ||
|---|---|---|
| तत्व | अभिकारक (LHS) | उत्पाद (RHS) |
| Fe | 1 | 2 |
| H | 3 × 2 = 6 | 2 |
| O | 1 x 3 = 3 | 3 |
चरण (4) रासायनिक समीकरण में इस संशोधन के बाद हम पाते हैं कि अभिकारक में वर्तमान जल के अणु में हाइड्रोजन की संख्या 6 (छ:) हो गयी है, जबकि उत्पाद में हाइड्रोजन के परमाणुओं की संख्या केवल 2 (दो) है।
अत: दोनों पक्षों में हाइड्रोजन के परमाणुओं की संख्या को संतुलित करने के लिए उत्पाद में वर्तमान H2 (हाइड्रोजन) को 3 (तीन) से गुणा करें जिससे हाइड्रोजन के परमाणुओं की संख्या 3 × 2 = 6 हो जायेगी, तथा दोनों पक्षों में बराबर हो जायेगी।
Fe⁄आयरन + 3H2O⁄जल → Fe2O3⁄आयरन (III) ऑक्साइड + 3H2⁄हाइड्रोजन
चरण (5) रासायनिक समीकरण को इस संशोधन के पश्चात अवलोकन से पता चलता है कि अभिकारक में आयरन (Fe) की संख्या 1 (एक) है, जबकि उत्पाद में वर्तमान Fe2O में आयरन (Fe) की संख्या 2 (दो) है।
अत: आयरन (Fe) की संख्या दोनों पक्षों में संतुलित करने के लिए, अभिकारक में वर्तमान आयरन (Fe) को 2 (दो) से गुणा करें।
2Fe⁄आयरन + 3H2O⁄जल → Fe2O3⁄आयरन (III) ऑक्साइड + 3H2⁄हाइड्रोजन
चरण (6) रासायनिक समीकरण में इस संशोधन के पश्चात, उसके दोनों पक्षों में वर्तमान तत्वों के परमाणुओं की संख्याओं को पुन: एक टेबल में लिखकर उनका अवलोकन करें।
| दोनों पक्षों में परमाणुओं संख्या | ||
|---|---|---|
| तत्व | अभिकारक (LHS) | उत्पाद (RHS) |
| Fe | 2 | 2 |
| H | 3 x 2 = 6 | 2 x 3 = 6 |
| O | 1 x 3 = 3 | 3 |
अब उपरोक्त टेबल के अवलोकन से पता चलता है कि संशोधन के पश्चात दिये गये रासायनिक समीकरण के दोनों पक्षों में वर्तमान तत्वों के परमाणुओं की संख्या बराबर हो गयी है। अत: दिया गया रासायनिक समीकरण संतुलित हो गया है।
Reference: