धातु एवं अधातु - क्लास दसवीं विज्ञान
Back to 10th-science-home(Hindi)
NCERT पाठ अंतर्गत प्रश्नों के उत्तर
प्रश्न संख्या: 1. ऐसी धातु का उदाहरण दीजिए जो
(i) कमरे के ताप पर द्रव होती है।
उत्तर: मरकरी (Hg)
ब्याख्या: मरकरी ही एक ऐसा धातु है जो कि कमरे के ताप पर द्रव होता है, बाकि सभी धातु ठोस होते हैं। मरकरी एक अपवाध है।
(ii) चाकू से आसानी से काटा जा सकता है।
उत्तर: सोडियम (Na)
ब्याख्या: धातु कठोर होते हैं, परंतु सोडियम ऐसा धातु है, जो कठोर नहीं है, यह इतना मुलायम है कि इसे चाकू से आसानी से काटा जा सकता है।
(iii) उष्मा की सबसे अच्छी चालक होती है।
उत्तर: सिल्वर (चाँदी)
ब्याख्या: सभी धातु उष्मा तथा विद्युत का चालक होता है, परंतु सभी धातुओं में सिल्वर सबसे अच्छा चालक है, परंतु सिल्वर के अधिक मँहगा होने के कारण इसका उपयोग बिजली के तार बनाने में नहीं किया जाता है। ताँबा, एलुमिनियम भी धातु है, तथा उष्मा तथा विद्युत का चालक है। यही कारण बिजली के तार तथा बर्तन बनाने में ताँबा तथा ऐलुमिनियम का उपयोग किया जाता है।
(iv) उष्मा की कुचालक होती है।
उत्तर: लेड (Lead)
ब्याख्या: सभी धातु उष्मा का चालन करती है, परंतु लेड एक ऐसा धातु है जो उष्मा का कुचालक होता है।
प्रश्न संख्या: 2. अघातवर्घ्य तथा तन्य का अर्थ बताइए।
उत्तर:
अघातवर्ध्य : धातुओं को पीटकर पतले चादर में बदला जा सकता है। धातु के इस गुण को अघातवर्धनीयता (Malleability) कहा जाता है, तथा धातुओं अघातवर्ध्य कहा जाता है।
इसी कारण से लोहे का उपयोग वाहनों के बॉडी को बनाने में होता है, तथा ऐलुमिनियम, ताँबा आदि का उपयोग बर्तन बनाने के काम में होता है। बर्तन या वाहनों के बॉडी के निर्माण से पहले धातुओं को पतले चादर के रूप में बदला जाता है।
तन्य: धातुओं को खींचकर पतले तार में बदला जा सकता है। धातुओं के इस गुण को तन्यता या लचीलापन (Ductility) कहा जाता है तथा धातुओं को तन्य कहा जाता है।
उदारण: ऐलुमिनियम तथा ताँबा, जो कि धातु हैं, का उपयोग बिजली के तार बनाने में किया जाता है।
प्रश्न संख्या: 3. सोडियम को किरोसीन में डुबो कर क्यों रखा जाता है?
उत्तर: सोडियम एक अत्यंत ही अभिक्रियाशील धातु है। यह जल के साथ बहुत तेजी से प्रतिक्रिया करता है। सोडियम वायु में वर्तमान जलवाष्प के कणों से भी प्रतिक्रिया करता है।
अत: सोडियम को वायु में वर्तमान जल के कणों से प्रतिक्रिया को रोकने तथा जल के साथ प्रतिक्रिया की किसी अप्रत्याशित दुर्घटना से बचने के लिए सोडियम को केरोसीन में डुबो कर रखा जाता है। सोडियम केरोसीन से प्रतिक्रिया नहीं करता है।
प्रश्न संख्या: 4. इन अभिक्रियाओं के लिए समीकरण लिखिए:
(i) भाप के साथ आयरन
उत्तर:
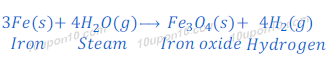
(ii) जल के साथ कैल्शियम तथा पोटैशियम
उत्तर:
कैल्शियम का जल के साथ प्रतिक्रिया
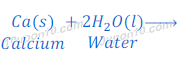
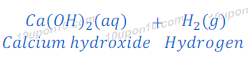
पोटैशियम का जल के साथ प्रतिक्रिया
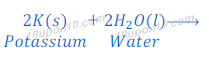
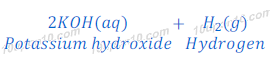
प्रश्न संख्या: 5. A, B, C एवं D चार धातुओं के नमूनों को लेकर एक एक करके निम्न विलयन में डाला गया। इससे प्राप्त परिणाम निम्न प्रकार से सारणीबद्ध किया गया है:
| धातु | आयरन (II) सल्फेट | कॉपर (II) सल्फेट | जिंक सल्फेट | सिल्वर नाइट्रेट |
|---|---|---|---|---|
| A | कोई अभिक्रिया नहीं | विस्थापन | ||
| B | विस्थापन | कोई अभिक्रिया नहीं | ||
| C | कोई अभिक्रिया नहीं | कोई अभिक्रिया नहीं | कोई अभिक्रिया नहीं | विस्थापन |
| D | कोई अभिक्रिया नहीं | कोई अभिक्रिया नहीं | कोई अभिक्रिया नहीं | कोई अभिक्रिया नहीं |
इस सारणी का उपयोग कर धातु A, B, C एवं D के संबंध में निम्न प्रश्नों के उत्तर दीजिए:
(i) सबसे अधिक क्रियाशील धातु कौन सी है?
उत्तर: B सबसे अधिक क्रियाशील धातु है।
(ii) धातु B को कॉपर(II) सल्फेट के विलयन में डाला जाए तो क्या होगा?
उत्तर: चूँकि B सबसे अधिक क्रियाशील धातु है, अत: जब B को कॉपर (II) सल्फेट के विलयन में डाला जायेगा तो B कॉपर को विस्थापित कर देगा।
(iii) धातु A, B, C तथा D को अभिक्रियाशीलता के घटते हुए क्रम में व्यवस्थित कीजिए।
उत्तर: B > A > C > D
प्रश्न संख्या: 6. अभिक्रियाशील धातु को तनु हाइड्रोक्लोरिक अम्ल में डाला जाता है तो कौन सी गैस निकलती है? आयरन के साथ तनु `H_2SO_4` की रासायनिक अभिक्रिया लिखिए।
उत्तर: जब अभिक्रियाशील धातु को तनु हाइड्रोक्लोरिक अम्ल में डाला जाता है, तो हाइड्रोजन गैस निकलती है।
उदारण: जब जिंक को तनु हाइड्रोक्लोरिक अम्ल में डाला जाता है, तो हाइड्रोजन गैस निकलती है, तथा जिंक सल्फेट (ZnSO4) बनता है।

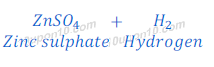
आयरन के साथ तनु `H_2SO_4` की रासायनिक अभिक्रिया
जब आयरन को तनु सल्फ्युरिक अम्ल (`H_2SO_4`) के साथ अभिक्रिया कराया जाता है, तो हाइड्रोजन गैस निकलती है, तथा आयरन सल्फेट बनता है।
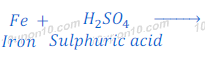
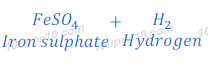
प्रश्न संख्या: 7. जिंक को आयरन (II) सल्फेट के विलयन में डालने से क्या होता है? इसकी रासायनिक अभिक्रिया लिखिए।
उत्तर: जिंक को आयरन (II) सल्फेट के विलयन में डालने पर जिंक धातु आयरन को विस्थापित कर देता है, तथा जिंक सल्फेट (`ZNSO_4`) बनाता है।

ऐसा जिंक धातु के आयरन से अधिक अभिक्रियाशील होने के कारण होता है। इस तरह की अभिक्रिया को विस्थापन अभिक्रिया (Displacement Reaction) कहते हैं।
प्रश्न संख्या: 8. (i) सोडियम, ऑक्सीजन एवं मैग्नीशियम के लिए इलेक्ट्रॉन बिन्दु संरचना लिखिए।
उत्तर: (i)
सोडियम [ Sodium (11)] की बिन्दु संरचना
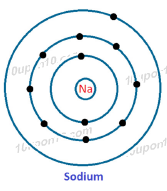
ऑक्सीजन [Oxygen (8)] की बिन्दु संरचना
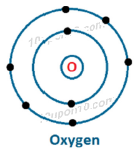
मैग्नीशियम [Magnesium (12)] की बिन्दु संरचना
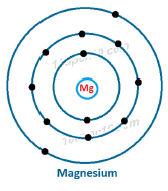
(ii) इलेक्ट्रॉन के स्थानांतरण के द्वारा `Na_2O` एवं `MgO` का निर्माण दर्शाइए।
(अ) इलेक्ट्रॉन के स्थानांतरण के द्वारा Na2 का निर्माण
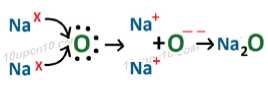
(ब) इलेक्ट्रॉन के स्थानांतरण के द्वारा MgO का निर्माण
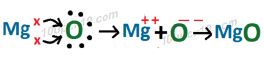
(iii) इन यौगिकों में कौन से आयन उपस्थित हैं?
सोडियम ऑक्साइड (Na2O) में सोडियम आयन तथा ऑक्साइड आयन उपस्थित होते हैं।
मैग्निशियम ऑक्साइड [Magnesium oxide(MgO)] में मैग्निशियम आयन तथा ऑक्साइड आयन उपस्थित होते हैं।
प्रश्न संख्या: 9. आयनिक यौगिकों का गलनांक उच्च क्यों होता है?
उत्तर: आयनिक यौगिकों का निर्माण आयनिक बंध के बनने के कारण होता है, अर्थात आयनिक यौगिकों के परमाणु आयनिक बंध के कारण जुड़े होते हैं। आयनिक बंध का वैद्युत आकर्षण बल काफी अधिक होता है, जिससे वे परमाणुओं को आपस में जोड़े रहते हैं तथा आयनिक बंध काफी मजबूत होते हैं।
आयनिक बंध के काफी मजबूत होने के कारण इसके वैद्युत आकर्षण बल को तोड़ने में काफी उर्जा की आवश्यकता होती है।
यही कारण है कि आयनिक यौगिकों का गलनांक उच्च होता है।
प्रश्न संख्या: 10. निम्न पदों की परिभाषा दीजिए:
(i) खनिज
उत्तर: तत्व (element) या यौगिक (compound) जो पृथ्वी की भूपर्पटी (earth's crust) में पाये जाते हैं को खनिज (Minerals) कहते हैं।
(ii) अयस्क
उत्तर: खनिज (Minerals) जिनमें किसी विशेष धातु या तत्व की मात्रा ज्यादा होती है तथा उन धातुओं या तत्वों को लाभकारी रूप से निकाला जा सकता है, अयस्क (Ores) कहते हैं।
(iii) गैंग
उत्तर: पृथ्वी की भूपर्पटी (earth's crust) से प्राप्त अयस्क (ores) में पाई जाने वाली अशुद्धियाँ यथा मिट्टी, बालू आदि, गैंग (Gangue) कहलाती है।
धातु के अयस्क (ores) से निष्कर्षण (Extraction) के पूर्व इन अशुद्धियों [गैंग (Gangue)] को हटाया जाता है।
प्रश्न संख्या: 11. दो धातुओं के नाम बताइए जो प्रकृति में मुक्त अवस्था में पाई जाती हैं।
उत्तर: सोना तथा चाँदी। सोना तथा चाँदी के काफी कम अभिक्रियाशील होने के कारण ये धातुएँ प्रकृति में मुक्त अवस्था में पाई जाती हैं।
प्रश्न संख्या: 12. धातु को उसके ऑक्साइड से प्राप्त करने के लिए किस रासायनिक प्रक्रम का उपयोग किया जाता है?
उत्तर: धातु को उसके ऑक्साइड से प्राप्त करने के लिए अवकरण् या उपचयन (Reduction) नामक रासायनिक प्रक्रम का उपयोग किया जाता है।
भर्जन (Roasting) या निस्तापन (Calcination) के बाद प्राप्त धातु के ऑक्साईड उपयुक्त उपाचय के साथ मिलाकर गर्म किया जाता है, जिससे धातु के ऑक्साईड संबंधित धातु में अवकरित हो जाता है। इस प्रक्रिया को अवकरण् या उपचयन कहा जाता है।
उदारण:
जिंक ऑक्साईड (Zinc oxide) से जिंक धातु प्राप्त करने के लिय अवकरण (Reduction)
भर्जन (Roasting) या निस्तापन (Calcination) के बाद प्राप्त जिंक ऑक्साईड [Zinc oxide(ZnO)] से अवकरण (Reduction) की विधि द्वारा जिंक (Zinc) धातु प्राप्त किया जाता है। इस प्रक्रिया में जिंक ऑक्साईड [Zinc oxide(ZnO)] को एक उपाचय (Reducing agent), यथा कार्बन (carbon) के साथ गर्म किया जाता है , जिससे जिंक ऑक्साईड [Zinc oxide(ZnO)] जिंक धातु (Zinc metal) में अवकरित (Reduced) हो जाता है।
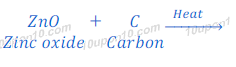
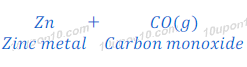
प्रश्न संख्या: 13. जिंक, मैग्नीशियम एवं कॉपर के धात्विक ऑक्साइडों को निम्न धातुओं के साथ गर्म किया गया:
| धातु | जिंक | मैग्नीशियम | कॉपर |
|---|---|---|---|
| जिंक ऑक्साइड | |||
| मैग्नीशियम ऑक्साइड | |||
| कॉपर ऑक्साइड |
किस स्थिति में विस्थापन अभिक्रिया घटित होगी?
उत्तर:
| धातु | जिंक | मैग्नीशियम | कॉपर |
|---|---|---|---|
| जिंक ऑक्साइड | कोई प्रतिक्रिया नहीं | विस्थापन | कोई प्रतिक्रिया नहीं |
| मैग्नीशियम ऑक्साइड | कोई प्रतिक्रिया नहीं | कोई प्रतिक्रिया नहीं | कोई प्रतिक्रिया नहीं |
| कॉपर ऑक्साइड | विस्थापन | विस्थापन | कोई प्रतिक्रिया नहीं |
(i) जब जिंक ऑक्साइड को मैग्निशियम के साथ गर्म किया जाता है, तो मैग्निशियम ज़िंक को विस्थापित कर देता है, तथा मैग्नीशियम ऑक्साइड बनाता है। 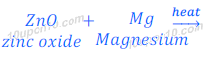
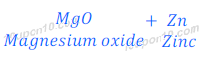
ऐसा मैग्नीशियम के जिंक से ज्यादा अभिक्रियाशील होने के कारण होता है।
(ii) जब जिंक ऑक्साइड को जिंक या कॉपर के साथ गर्म करने पर कोई अभिक्रिया नहीं होती है।
(iii) जब कॉपर ऑक्साइड को जिंक के साथ गर्म किया जाता है, तो जिंक के ज्यादा अभिक्रियाशील होने के कारण यह कॉपर को विस्थापित कर देता है तथा जिंक ऑक्साइड बनाता है।
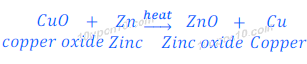
(iv) जब कॉपर ऑक्साइड को मैग्नीशियम के साथ गर्म किया जाता है, तो मैग्नीशियम कॉपर को विस्थापित कर देता है, तथा मैग्नीशियम ऑक्साइड बनता है। ऐसा मैग्नीशियम के कॉपर से ज्यादा अभिक्रियाशील होने के कारण होता है।
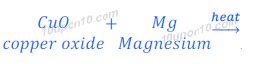
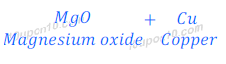
प्रश्न संख्या: 14. कौन सी धातु आसानी से संक्षारित नहीं होती है?
उत्तर: कॉपर, सिल्वर, तथा सोना आसानी से संक्षारित नहीं होती है, क्योंकि ये धातुएँ बहुत ही कम अभिक्रियाशील होते हैं।
प्रश्न संख्या: 15. मिश्रातु क्या होते हैं?
उतर: दो या दो से अधिक धातुओं के समांगी मिश्रण को मिश्रातु कहते हैं। इसे तैयार करने के लिए पहले मूल धातु को गलित अवस्था में लाया जाता है एवं तत्पश्चात दूसरे तत्वों को एक निश्चित अनुपात में इसमें विलीन किया जाता है। फिर इसे कमरे के ताप पर शीतलीकृत किया जाता है।
उदारण: स्टेनलेश स्टील एक मिश्रातु है, जिसे लोहा, क्रोमियम तथा निकेल धातुओं को मिलाने से बनाया जाता है।
ब्रांज एक मिश्रातु है, जिसे कॉपर तथ टिन को मिलाने से बनाया जाता है।
ब्रास एक मिश्रातु है, जिसे कॉपर तथा जिंक को मिलाकर बनाया जाता है।
Reference: