अम्ल, भस्म तथा लवण - क्लास दसवीं विज्ञान
Back to 10th-science-home(Hindi)
NCERT पाठ अंतर्गत प्रश्नों के हल
प्रश्न संख्या : 1.आपको तीन परखनलियाँ दी गई हैं। इनमें से एक में असावित जल एवं दो में से एक में अम्लीय विलयन तथा दूसरे में क्षारीय विलयन है। यदि आपको केवल लाल लिटमस पत्र दिया जाता है तो आप प्रत्येक परखनली में रखे गये पदार्थों की पहचान कैसे करेंगे?
उत्तर : अम्लीय घोल ब्लू लिटमस पत्र को लाल रंग में बदल देता है, तथा क्षारीय विलयन लाल लिटमस पत्र को ब्लू में बदल देता है। अत: दिये गये एक लाल लिटमस पत्र की मदद से निम्नाकित तरीके से दिये गये विलयनों की पहचान की जा सकती है:
(a) दिये गये लाल लिटमस पेपर को परखनली में डुबायेंगे, जिस परखनली में लाल लिटमस पत्र ब्लू हो जायेगा वह विलयन क्षारीय है। तथा उस परखनली को अलग कर लेबल लगा दिया गया।
(b) अब दिया गया लिटमस पेपर ब्लू हो गया है। उसे बचे हुए दोनों परखनली में बारी बारी डुबाऐंगे। जिस परखनली में लिटमस पेपर लाल हो गया, वह विलयन अम्लीय है। तथा उस परखनली को लेबल लगाकर अलग कर दिया गया।
(c) तथा जिस परखनली में लिटमस पेपर के रंग में कोई परिवर्तन नहीं होता है, वह विलयन आसवित जल है।
प्रश्न संख्या : 2. पीतल एवं ताम्बे के बर्तनों में दही एवं खट्टे पदार्थ क्यों नहीं रखने चाहिए?
उत्तर : घातु अम्ल के साथ प्रतिक्रिया कर हाइड्रोजन गैस तथा संबंधित लवण बनाता है। ताम्बा (Copper) एक धातु (metal) है तथा पीतल (brass) ताम्बा का एक मिश्रातु (Alloy) है।
अत: दही, जिसमें लैक्टिक अम्ल होता है, को यदि पीतल या ताम्बे के बर्तन में रखा जाता है, तो वह प्रतिक्रिया कर संबंधित लवण तथा हाइड्रोजन गैस बनायेगा, जिससे दही खराब हो जायेगा।
यही कारण है कि दही को पीतल या ताम्बे के बर्तनों में नहीं रखा जाता है।
प्रश्न संख्या : 3. घातु के साथ अम्ल की अभिक्रिया होने पर सामान्यत: कौन सी गैस निकलती है? एक उदाहरण के द्वारा समझाइए। इस गैस की उपस्थिति की जाँच आप कैसे करेंगे?
उत्तर : घातु अम्ल के साथ प्रतिक्रिया कर हाइड्रोजन गैस तथा संबंधित लवण बनाता है।
उदारहण: जब मैग्नीसियम धातु हाइड्रोक्लोरिक अम्ल के साथ प्रतिक्रिया करता है, तो हाइड्रोजन गैस तथा मैग्नीसियम क्लोराइड बनता है।

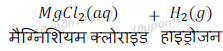
हाइड्रोजन गैस की जाँच:
हाइड्रोजन गैस एक पॉप आवाज के साथ जलती है।
अत: जब दिये गये अभिक्रिया में पाइप से निकलने वाली गैस के पास जलती हुई माचिस की तीली या मोमबत्ती को ले जाते हैं, तो वह पॉप आवाज के साथ जलने लगती है। यह बतलाता है, कि निकलने वाली गैस हाइड्रोजन है।
प्रश्न संख्या : 4. कोई धातु यौगिक 'A' तनु हाइड्रोक्लोरिक अम्ल के साथ अभिक्रिया करता है तो बुदबुदाहट उत्पन्न होती है। इससे उत्पन्न गैस जलती मोमबत्ती को बुझा देती है। यदि उत्पन्न यौगिकों में एक से कैल्सियम क्लोराइड हैं, तो इस अभिक्रिया के लिए संतुलित रासायनिक समीकरण लिखिए।
उत्तर : चूँकि उत्पन्न यौगिकों में एक कैल्सियम क्लोराइड (एक लवण) है, तथा निकलने वाली गैस मोमबत्ती को बुझा देती है, अत: निकलने वाली गैस कार्बन डाइऑक्साइड है, जो कि आग बुझाने के काम आता है।
अर्थात अभिकारक कैल्सियम कार्बोनेट तथा हाइड्रोक्लोरिक अम्ल है।
जब कैल्सियम कार्बोनेट हाइड्रोक्लोरिक अम्ल के साथ प्रतिक्रिया करता है, तो बुदबुदाहट के साथ कार्बन डाइऑक्साइड गैस निकलती है तथा कैल्सियम कार्बोनेट बनता है।
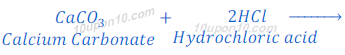
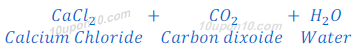
अत: यौगिक 'A' कैल्सियम कार्बोनेट है।
प्रश्न संख्या : 5. HCl, HNO3 आदि जलीय विलयन में अम्लीय अभिलक्षण प्रदर्शित करते हैं, जबकि ऐल्कोहॉल एवं ग्लूकोज जैसे यौगिकों के विलयनों में अम्लीयता के अभिलक्षण नहीं प्रदर्शित होते हैं?
उत्तर : एक अम्ल जलीय घोल में हाइड्रोजन आयन dissociate (अलग करना या देना) करने के कारण अम्लीय अभिलक्षण प्रदर्शित करता है।
चूँकि HCl, HNO3 आदि जलीय विलयन में हाइड्रोजन आयन देता है। जबकि ऐल्कोहॉल तथा ग्लूकोज जैसे यौगिकों में हाइड्रोजन होने के बाबजूद भी जलीय घोल में ये हाइड्रोजन आयन नहीं देते हैं या अलग करते हैं।
अत: HCl, HNO3 आदि जलीय विलयन में अम्लीय गुण प्रदर्शित करते हैं तथा ऐल्कोहॉल तथा ग्लूकोज जैसे यौगिक जलीय विलयन में अम्लीयता के अभिलक्षण नहीं प्रदर्शित करते हैं।
प्रश्न संख्या : 6. अम्ल का जलीय विलयन क्यों विद्युत का चालन करता है?
उत्तर : जल में उपस्थित अशुद्धियों के रूप में वर्तमान लवणों के आयन के रूप में उपस्थित होने के कारण ही विद्युत के चालन होता है। चूँकि आसवित जल में कोई भी लवण नहीं होता है, अत: आसवित जल में विद्युत का चालन नहीं होता है।
अम्ल जलीय विलयन में अपने संबंधित हाइड्रोजन आयन तथा हाइड्रोक्साइड आयन में टूट जाता है। अम्ल के जलीय विलयन में आयनों के वर्तमान होने के कारण ही वह विद्युत का चालन करता है।
प्रश्न संख्या : 7. शुष्क हाइड्रोक्लोरिक गैस शुष्क लिटमस पत्र के रंग को क्यों नहीं बदलती है?
उत्तर : कोई भी अम्ल हाइड्रोजन आयन की उपस्थिति के कारण ही अम्लीय अभिलक्षण प्रदर्शित करता है। तथा एक अम्ल जलीय विलयन में हाइड्रोजन आयन देता है।
चूँकि शुष्क हाइड्रोक्लोरिक गैस में जल की अनुपस्थिति के कारण हाइड्रोजन आयन वर्तमान नहीं होता है, अत: शुष्क हाइड्रोक्लोरिक गैस शुष्क लिटमस पत्र के रंग को नहीं बदलती है।
वहीं जल से गीले लिटमस ब्लू लिटमस पत्र को शुष्क हाइड्रोजन गैस लाल रंग में बदल देता है।
प्रश्न संख्या : 8. अम्ल को तनुकृत करते समय यह क्यों अनुशंसित करते हैं कि अम्ल को जल में मिलाना चाहिए न कि जल को अम्ल में?
उत्तर : अम्ल में जल मिलाना या जल में अम्ल मिलाना एक उष्माक्षेपी अभिक्रिया (Exothermic Reaction) है।
यदि अम्ल में जल मिलाया जाता है, तो उससे बहुत अधिक उष्मा उत्सर्जित होती है, जिससे अम्ल उछलकर हाथों आदि पर पड़्कर जला सकता है या और ज्यादा खतरनाक हो सकता है। जबकि तनुकृत करने के लिए जल में धीरे धीरे अम्ल मिलाने पर उत्सर्जित होने वाली उष्मा की मात्रा जल की अधिकता के कारण अवशोषित हो जाती है।
अत: यह अनुशंसित किया जाता है कि अम्ल को तनुकृत करने के लिए अम्ल में जल नहीं बल्कि जल में अम्ल को धीरे धीरे मिलाया जाता है।
प्रश्न संख्या : 9. अम्ल के विलयन को तनुकृत करते समय हाइड्रोनियम आयन (H3O+) की सांद्रता कैसे प्रभावित हो जाती है?
उत्तर : हम जानते हैं कि विलयन की सान्द्रता = विलेय की मात्रा / विलयन की मात्रा। अर्थात विलयन की सान्द्रता विलेय की निश्चित मात्रा पर विलयन की मात्रा बढ़ने पर धटती है, तथा विलयन की मात्रा घटने पर बढ़ती है।
अत: अम्ल के विलयन को तनुकृत करने पर जल अर्थात विलयन की मात्रा अधिक हो जाने के कारण विलयन की सान्द्रता अर्थात हाइड्रोनियम आयन (H3O+) की सान्द्रता घट जाती है।
प्रश्न संख्या : 10 . जब सोडियम हाइड्रॉक्साइड विलयन में आधिक्य क्षारक मिलाते हैं तो हाइड्रॉक्साइस आयन (OH–) की सांद्रता कैसे प्रभावित होती है?
उत्तर : क्षारक विलयन हाइड्रॉक्साइस आयन (OH–) मुक्त करता है। चूँकि सोडियम हाइड्रोक्साइड एक क्षार है, अत: सोडियम हाइड्रोक्साइड के विलयन में हाइड्रॉक्साइस आयन (OH–) मुक्त अवस्था में वर्तमान रहता है। जब उसमें क्षारक आधिक्य में मिलाते हैं तो हाइड्रॉक्साइड आयन (OH–) की सान्द्रता बढ़ जाती है।
प्रश्न संख्या : 11 . आपके पास दो विलयन 'A' एवं 'B' हैं। विलयन 'A' के पीoएचo (pH) का मान 6 है एवं विलयन 'B' के पीoएचo (pH) का मान 8 है| किस विलयन में हाइड्रोजन आयन की सांद्रता अधिक है? इनमें से कौन अम्लीय है तथा कौन क्षारकीय?
उत्तर : पीoएचo (pH) स्केल 1 से 14 के मान पर कार्य करता है। इसमें पीoएचo (pH) का मान 7 (सात) उदासीन विलयन को दर्शाता है। विलयन जिसके पीoएचo (pH) का मान 7 (सात) से कम होता है, वह अम्लीय तथा जिसके पीoएचo (pH) का मान 7 (सात) से अधिक होता है क्षारीय होता है।
चूँकि दिये गये विलयन 'A' के पीoएचo (pH) का मान 6 है, जो 7 (सात) से कम है, अत: विलयन 'A' अम्लीय है।
तथा विलयन 'B' के पीoएचo (pH) का मान 8 है, जो कि 7 (सात) से अधिक है, अत: विलयन 'B' क्षारीय है।
प्रश्न संख्या : 12 . H+ (aq) आयन की सांन्द्रता का विलयन की प्रकृति पर क्या प्रभाव पड़ता है?
उत्तर : H+ (aq) आयन की सांन्द्रता बढ़ने पर विलयन में अम्लीयता बढ़ती है तथा H+ (aq) आयन की सांन्द्रता घटने पर विलयन की क्षारकता बढ़ती है।
प्रश्न संख्या : 13 . क्या क्षारकीय विलयन में H+ (aq) आयन होते हैं? यदि हाँ, तो क्षारकीय क्यों होते हैं?
उत्तर : हाँ क्षारकीय विलयन में H+ (aq) आयन होते हैं।
जिस विलयन में H+ (aq) आयन की सान्द्रता अधिक होती है वह अम्लीय तथा जिस विलयन में हाइड्रॉक्साइड आयन (OH–) की सान्द्रता अधिक होती है, वह क्षारकीय होता है।
चूँकि क्षारकीय विलयन में हाइड्रॉक्साइड आयन (OH–) की सान्द्रता H+ (aq) आयन के सान्द्रता से अधिक होती है, अत: क्षारकीय विलयन में H+ (aq) आयन की उपस्थिति के बाबजूद भी वह क्षारकीय होता है।
प्रश्न संख्या : 14. कोई किसान खेत की मृदा की किस परिस्थिति में बिना बुझा हुआ चूना (कैल्सियम ऑक्साइड), बुझा हुआ चून (कैल्सियम हाइड्रोक्साइड) या चॉक (कैल्सियम कार्बोनेट) का उपयोग करेगा?
उत्तर : बिना बुझा हुआ चूना (कैल्सियम ऑक्साइड), बुझा हुआ चून (कैल्सियम हाइड्रोक्साइड) या चॉक (कैल्सियम कार्बोनेट) क्षारकीय होते हैं।
अत: कोई किसान खेत की मृदा के अम्लीय हो जाने की स्थिति में बिना बुझा हुआ चूना (कैल्सियम ऑक्साइड), बुझा हुआ चून (कैल्सियम हाइड्रोक्साइड) या चॉक (कैल्सियम कार्बोनेट) का उपयोग करके मृदा को उदासीन बनायेगा।
प्रश्न संख्या : 15 . CaOCl2 यौगिक का प्रचलित नाम क्या है?
उत्तर : CaOCl2 यौगिक का प्रचलित नाम विरंजक चूर्ण [ब्लीचिंग पाउडर (Bleaching Powder)] है।
प्रश्न संख्या : 16 . उस पदार्थ का नाम बताइए जो क्लोरीन से क्रिया करके विरंजक चूर्ण बनाता है।
उत्तर : कैल्सियम हाइड्रोक्साइड
जब कैल्सियम हाइड्रोक्साइड (Ca(OH)2) की अभिक्रिया क्लोरीन (Cl2) के साथ होती है, तो यह विरंजक चूर्ण (Bleaching Powder) बनाता है।
प्रश्न संख्या : 17 . कठोर जल को मृदु करने के लिए किस सोडियम यौगिक का उपयोग किया जाता है?
उत्तर : सोडियम कार्बोनेट [Washing Soda (Na2CO3)], जो कि सोडियम का एक यौगिक है का उपयोग कठोर जल को मृदु करने के लिए किया जाता है।
प्रश्न संख्या : 18 . सोडियम हाइड्रोजनकार्बोनेट के विलयन को गर्म करने पर क्या होगा? इस अभिक्रिया के लिए समीकरण लिखिए।
उत्तर : सोडियम हाइड्रोजन कार्बोनेट (Na2CO3) के विलयन को गर्म करने पर यह सोडियम कार्बोनेट, कार्बन डाइऑक्साइड गैस तथा जलवाष्प देता है।

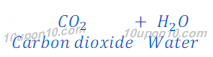
प्रश्न संख्या : 19 . प्लास्टर ऑफ पेरिस की जल के साथ अभिक्रिया के लिए समीकरण लिखिए।
उत्तर : प्लास्टर ऑफ पेरिस जल के साथ प्रतिक्रिया कर जिप्सम बनाता है।
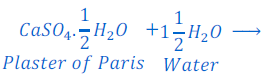
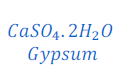
Reference: