अम्ल, भस्म तथा लवण - क्लास दसवीं विज्ञान
Back to 10th-science-home(Hindi)
NCERT अभ्यास प्रश्नों के हल
प्रश्न संख्या : 1 . कोई विलयन लाल लिटमस को नीला कर देता है, इसका pH संभवत: क्या होगा?
(a) 1
(b) 4
(c) 5
(d) 10
उत्तर : (d) 10
उत्तर : पीoएचo (pH) स्केल 1 से 14 के मान पर कार्य करता है। इसमें पीoएचo (pH) का मान 7 (सात) उदासीन विलयन को दर्शाता है। विलयन जिसके पीoएचo (pH) का मान 7 (सात) से कम होता है, वह अम्लीय तथा जिसके पीoएचo (pH) का मान 7 (सात) से अधिक होता है क्षारीय होता है।
चूँकि दिया गया विलयन लाल लिटमस पत्र को नीला कर देता है, अर्थात दिया गया विलयन क्षारीय है। अत: इसका पीoएचo (pH) का मान 7 (सात) से अधिक होगा।
अत: विकल्प (d) 10 सही उत्तर है।
प्रश्न संख्या : 2 . कोई विलयन अंडे के पिसे कवच से अभिक्रिया कर एक गैस उत्पन्न करता है जो चूने के पानी को दुधिया कर देती है। इस विलयन में क्या होगा?
(a) NaCl
(b) HCl
(c) LiCl
(d) KCl
उत्तर : (b) HCl
ब्याख्या : अंडे का कवच कैल्सियम कार्बोनेट का बना होता है।
जब कैल्सियम कार्बोनेट हाइड्रोक्लोरिक अम्ल के साथ प्रतिक्रिया करता है, तो कैल्सियम क्लोराइड तथा कार्बन डाइऑक्साइड गैस बनता है।
जब कार्बन डाइऑक्साइड गैस को चूने के पानी में पास करवाया जाता है, तो यह चूने के पानी को दुधिया कर देता है।
प्रश्न संख्या : 3 . NaOH का 10 mL विलयन, HCl के 8 mL विलयन से पूर्णत: उदासीन हो जाता है। यदि हम NaOH के उसी विलयन 20 mL लें तो इसे उदासीन करने के लिए HCl के उसी विलयन की कितनी मात्रा की अवश्यकता होगी?
(a) 4 mL
(b) 8 mL
(c) 12 mL
(d) 16 mL
उत्तर : (d) 16 mL
ब्याख्या : चूँकि NaOH का 10 mL विलयन को उदासीन करने के लिये HCl के 8 mL की आवश्यकता होती है। अत: चूँकि NaOH का (10 x 2=) 20 mL विलयन को उदासीन करने के लिये HCl के 8 × 2 = 16 mL की आवश्यकता होती है।
अत: Answer = (d) 16 mL
प्रश्न संख्या : 4 . अपच का उपचार करने के लिए निम्न में से किस औषधि का उपयोग होता है?
(a) एंटीबायोटिक (प्रतिजैविक)
(b) ऐनालसेजिक (पीड़ाहरी)
(c) एंटैसिड
(d) एंटीसेप्टिक (प्रतिरोधी)
उत्तर : (c) एंटैसिट
ब्याख्या : अधिक खा लेने के कारण उसके पाचन के लिए हमारा पेट अतिरिक्त हाइड्रोक्लोरिक अम्ल स्त्रावित करने लगता है, जिस कारण से अपच हो जाता है। अत: अतिरिक्त हाइड्रोक्लोरिक अम्ल को उदासीन करने के लिए एंटासिड (Antacid (अम्ल को उदासीन करने वाला)) नामक औषधि का उपयोग किया जाता है।
प्रश्न संख्या : 5 . निम्न अभिक्रिया के लिए पहले शब्द समीकरण लिखिए तथा उसके बाद संतुलित समीकरण लिखिए:
(a) तनु सल्फ्युरिक अम्ल दानेदार जिंक के साथ अभिक्रिया करता है।
उत्तर :
सल्फ्युरिक अम्ल + जिंक ⇒ जिंक क्लोराइड + हाइड्रोजन
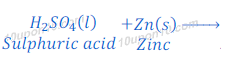
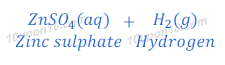
(b) तनु हाइड्रोक्लोरिक अम्ल मैग्नीशियम पट्टी के साथ अभिक्रिया करता है।
उत्तर :
सल्फ्युरिक अम्ल + मैग्नीशियम → मैग्नीशियम क्लोराइड + हाइड्रोजन
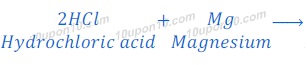

(c) तनु सल्फ्युरिक अम्ल ऐल्मुनियम चूर्ण के साथ अभिक्रिया करता है।
उत्तर :
सल्फ्युरिक अम्ल + एलुमिनियम → एलुमिनियम क्लोराइड + हाइड्रोजन

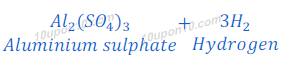
(d) तनु हाइड्रोक्लोरिक अम्ल लौह के रेतन के साथ अभिक्रिया करता है।
सल्फ्युरिक अम्ल + आयरन → आयरन क्लोराइड + हाइड्रोजन
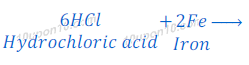
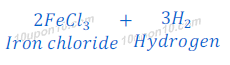
प्रश्न संख्या : 6 . ऐल्कोहॉल एवं ग्लूकोज जैसे यौगिकों में भी हाइड्रोजन होते हैं लेकिन इनका वर्गीकरण अम्ल की तरह नहीं होता है। एक क्रियाकलाप द्वारा इसे साबित कीजिए।
उत्तर : वैसा रासायनिक पदार्थ जो जल के विलयन में हाइड्रोजन आयन मुक्त करते हैं, का वर्गीकरण अम्ल के रूप में किया जाता है। चूँकि एल्कोहॉल एवं ग्लूकोज जल के विलयन में हाइड्रोजन आयन मुक्त नहीं करते हैं, अत: इनका वर्गीकरण अम्ल की तरह नहीं होता है। इसे निम्नलिखित क्रिया कलाप द्वारा साबित किया जा सकता है।
क्रियाकलाप:
आवश्यक सामग्री: दो परखनली, लाल तथा नीला लिटमस पेपर, ऐल्कोहॉल तथा ग्लूकोज
प्रक्रिया
दो साफ परखनली लेकर एक में एल्कोहॉल तथा दूसरे में ग्लूकोज का जलीय विलयन बना लिया जाता है, तथा लेबल लगा दिया जाता है।
दोनों विलयन में बारी बारी से नीला तथा लाल लिटमस पत्र डुबाया जाता है।
प्रेक्षण :
किसी भी परखनली का विलयन लिटमस पत्र के रंग को नहीं बदलता है।
निष्कर्ष:
चूँकि एल्कोहॉल एवं ग्लूकोज जल के विलयन में हाइड्रोजन आयन मुक्त नहीं करते हैं, अत: दोनों में से कोई भी नीले लिटमस पत्र को लाल रंग में नहीं बदलता है।
अत: कोई भी विलयन अम्ल नहीं है।
प्रश्न संख्या : 7 . आसवित जल विद्युत का चालक क्यों नहीं होता जबकि वर्षा जल होता है?
उत्तर : जल में उपस्थित अशुद्धियों के आयन विद्युत का संवहन या चालन करते हैं।
चूँकि आसवित जल में कोई अशुद्धि नहीं रहती है, तदनुसार कोई आयन भी उपस्थित नहीं रहता है, अत: आसवित जल विद्युत का चालन नहीं होता है, अर्थात आसवित जल विद्युत का चालक नहीं होता है।
वहीं बर्षा के जल में कई अशुद्धियाँ रहती हैं, जिनके आयन भी जल में मुक्त अवस्था में रहते हैं, जो कि विद्युत का चालन करते हैं।
अत: आसवित जल विद्युत का चालक नहीं होता है जबकि बर्षा का जल विद्युत का चालक होता है।
प्रश्न संख्या : 8 . जल की अनुपस्थिति में अम्ल का व्यवहार आम्लीय क्यों नहीं होता है?
उत्तर : अम्ल के विलयन में उपस्थित मुक्त अवस्था में हाइड्रोजन आयन ही अम्लीय व्यवहार के लिए उत्तरदायी होता है।
चूँकि जल की अनुपस्थिति में अम्ल में वर्तमान हाइड्रोजन, आयन के रूप में मुक्त अवस्था में नहीं रहता है, अत: जल की अनुपस्थिति में अम्ल का व्यवहार आम्लीय नहीं होता है।
प्रश्न संख्या : 9 . पाँच विलयनों A, B, C, D, व E की जब सार्वत्रिक सूचक से जाँच की जाती है तो pH के मान क्रमश: 4, 1, 11, 7 एवं 9 प्राप्त होते हैं। कौन सा विलयन:
(a) उदासीन है?
(b) प्रबल क्षारीय है?
(c) प्रबल अम्लीय है?
(d) दुर्बल अम्लीय है?
(e) दुर्बल क्षारीय है?
pH के मानों को हाइड्रोजन आयन की सांद्रता के आरोही क्रम में व्यवस्थित कीजिए।
उत्तर : पीoएचo (pH) स्केल 1 से 14 के मान पर कार्य करता है। इसमें पीoएचo (pH) का मान 7 (सात) उदासीन विलयन को दर्शाता है। विलयन जिसके पीoएचo (pH) का मान 7 (सात) से कम होता है, वह अम्लीय तथा जिसके पीoएचo (pH) का मान 7 (सात) से अधिक होता है क्षारीय होता है।
अत: (a) विलयन (D) जिसके पीoएचo (pH) का मान 7 (सात) है उदासीन है।
(b) विलयन (C) जिसके पीoएचo (pH) का मान 11 (ग्यारह) है, प्रबल क्षारीय है।
(c) विलयन (B) जिसके पीoएचo (pH) का मान 1 (एक) है, प्रबल अम्लीय है।
(d) विलयन (A) जिसके पीoएचo (pH) का मान 4 (चार) है, दुर्बल अम्लीय है।
(e) विलयन (E) जिसके पीoएचo (pH) का मान 9 (नौ) है, दुर्बल क्षारीय है।
दिये गये विलयनो की pH के मानो तथा हाइड्रोजन आयन की सान्द्रता के आधार पर आरोही क्रम:
C < E < D < A < B
प्रश्न संख्या : 10 . परखनली 'A' एवं 'B' में समान लम्बाई की मैग्निशियम की पट्टी लीजिए। परखनली 'A' में हाइड्रोक्लोरिक अम्ल (HCl) तथा परखनली 'B' में ऐसिटिक अम्ल (CH3COOH) डालिए। किस परखनली में अधिक तेजी से बुदबुदाहट होगी तथा क्यों?
उत्तर : चूँकि परखनली (A) में रखा गया हाइड्रोक्लोरिक अम्ल एक प्रबल अम्ल है जबकि परखनली (B) में रखा गया ऐसिटिक अम्ल एक दुर्बल अम्ल है और एक प्रबल अम्ल ज्यादा प्रबल रूप से अभिक्रिया करता है।
अत: परखनली (A) में परखनली (B) की अपेक्षा अधिक तेजी से बुदबुदाहट होगी।
प्रश्न संख्या : 11 . ताजे दूध के pH का मान 6 होता है। दही बन जाने पर इसके pH के मान में क्या परिवर्तन होगा? अपना उत्तर समझाइए।
उत्तर : दूध तथा दही दोनों में लैक्टिक अम्ल पाया जाता है। परंतु दही में लैक्टिक अम्ल की सांद्रता अधिक रहती है, जबकि दूध में कम। इसी कारण दही का स्वाद खट्टा होता है।
अत: दही बन जाने पर उसके pH का मान ताजे दूध के मान (6) से कम हो जायेगा चूँकि अम्लीयता बढ़ने पर pH (पीoएचo) का मान घटता है।
प्रश्न संख्या : 12 . एक ग्वाला ताजे दूध में थोड़ा बेकिंग सोडा मिलाता है।
(a) ताजा दूध के pH के मान को 6 से बदलकर थोड़ा क्षारीय क्यों बना देता है?
उत्तर : दूध में वर्तमान बैक्टीरिया जैविक क्रियाओं के कारण दूध की अम्लीयता बढ़ा देते हैं, जिसके कारण दूध दही के रूप में बदल जाता है। परंतु यदि दूध को थोड़ा क्षारीय बना दिया जाय तो बैक्टीरिया द्वारा की जाने वाली जैविक क्रिया धीमी हो जाती है, तथा दूध की अम्लीयता बढ़ने में देर लगती है।
अत: एक ग्वाला थोड़ा बेकिंग सोडा, जो कि एक क्षार है, को मिलाकर ताजे दूध के pH के मान को 6 से बदलकर थोड़ा क्षारीय बना देता है, ताकि दूध अधिक देर तक नहीं खराब हो, अर्थात दही में नहीं बदले।
(b) इस दूध को दही बनने में अधिक समय क्यों लगता है?
उत्तर : ताजे दूध में थोड़ा बेकिंग सोडा मिला देने पर दूध में वर्तमान बैक्टीरिया द्वारा की जाने वाली जैविक प्रक्रिया धीमी पड़ जाती है, तथा दूध की अम्लीयता बढ़ने में समय लगता है, जिसके कारण इस दूध को दही बनने में अधिक समय लगता है।
प्रश्न संख्या : 13 . प्लास्टर ऑफ पेरिस को आर्द्र-रोधी बर्तन में क्यों रखा जाना चाहिए। इसकी ब्याख्या किजिए।
उत्तर : जब प्लास्टर ऑफ पेरिस हवा के संपर्क में आता है, तो हवा में नमी के रूप में वर्तमान जल से अभिक्रिया कर जिप्सम, जो कि कठोर होता है, में बदल जाता है।
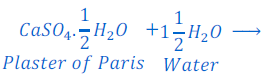
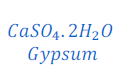
अत: प्लास्टर ऑफ पेरिस को ठोस के रूप में जमने से बचाने के लिए उसे आर्द्ररोधी बर्तन में रखा जाता है।
प्रश्न संख्या : 14 . उदासीनीकरण अभिक्रिया क्या है? दो उदाहरण दीजिए।
उत्तर : अम्ल का क्षार के साथ प्रतिक्रिया कर एक दूसरे को उदासीन बनाने की अभिक्रिया उदासीनीकरण अभिक्रिया कहलाता है।
जब अम्ल एक क्षार के साथ अभिक्रिया करता है, तो दोनों एक दूसरे को उदासीन कर देता है, तथा सबंधित लवण और जल बनता है। यह अभिक्रिया उदासीनीकरण अभिक्रिया भी कहलाता है।
उदारण : (1) : जब हाइड्रोक्लोरिक अम्ल सोडियम हाइड्रोक्साइड (एक क्षार) के साथ अभिक्रिया करता है, तो सोडियम क्लोराइड (नमक) तथा जल बनता है।
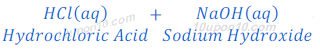
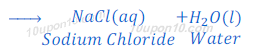
उदाहरण : (2) : जब सल्फ्युरिक अम्ल सोडियम हाइड्रोक्साइड के साथ अभिक्रिया करता है, तो सोडियम सल्फेट तथा जल बनता है।
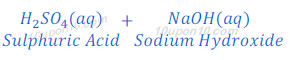
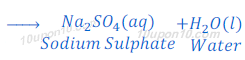
प्रश्न संख्या : 15 . धोने का सोडा एवं बेकिंग सोडा के दो-दो प्रमुख उपयोग बताइए।
उत्तर :
(अ) धोने का सोडा [Sodium carbonate (Na2CO3)] के उपयोग:
कपड़े को धोने में
जल की कठोरता को दूर करने में
(ब) बेकिंग सोडा के उपयोग:
बेकरी में आटे या मैदा को मुलायम बनाने में
आग बुझाने वाले संयंत्र में एक घटक से रूप में
Reference: